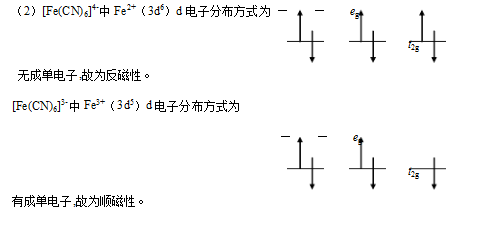
fe(cn)6 3- 为什么有顺磁性 fe高温下的晶格类型
用价键理论解释六水合铁是顺磁性的,配位化合物的内外轨型和顺逆磁性,为什么课本上说内轨型的是逆磁性,逆磁性不是应该无成单电子吗?[Fe(H2O)6]2+为顺磁性,而[Fe(CN)6)]4-为反磁性,请分别用价键理论和晶体场理..,)[Fe(CN)6]4-为反磁性,而[Fe(CN)6]3-为顺磁性,为什么?[Fe(CN)6]4-为反磁性,而[Fe(CN)6]3-为顺磁性,为什么?[Fe(CN)6]3-有磁矩而[Fe(CN)6]4-的磁矩却为零,为什么?
本文导航
六价铁离子结构示意图
阳午,你好!你讲的是【Fe(H2O)6】3+或【Fe(H2O)6】2+吧!他们都是水合离子,即以水为配体的配合物!可用配位场理论和晶体场理论均可解决。
1、由于H2O是弱场(在此处是6个配体点点和构成的正八面体Oh静电场,),Fe的d5 5个轨道分裂成两组即eg和T2g轨道,因为H2O是弱场配体,即裂分Fe的d轨道分裂能较(成对能)小!因此Fe3+ 5个裂分后的d轨道中各有一个单电子;而Fe2+5个裂分后的d轨道中共6个电子,即有4个单电子.因为有单电子,所以是顺磁性物质!
当然,如果遇到了CN-这样的暴君---强场配体,它使Fe2+的6个价电子都挤在三个T2g轨道中,而显抗磁性!而Fe3+因尚有一个孤电子仍然表现顺磁性!!
只要肯登攀,化学很简单!
祝进步!
顺磁性和抗磁性怎么判断
首先,没有[Fe(CN)6]3+,只有[Fe(CN)6]3-和[Fe(CN)6]4-,课本上没有说[Fe(CN)6]3-是逆磁性,而只说了[Fe(CN)6]4-是逆磁性。
内外轨型与顺逆磁性没有绝对关系,只是内轨型的磁矩要小一些。
希望对你有所帮助!
望采纳!
fe高温下的晶格类型
顺磁性表示此物质中有未成对的电子,反磁表示电子全部成对。Fe(II) 电子组态:3d6
价键理论:
[Fe(H2O)6]2+ [Fe(CN)6)]4-
杂化: sp3d2 d2sp3
未成对电子数: 4 0
晶体场理论:
弱场 (高自旋) 强场 (低自旋)
电子排布: (t2g)4(eg)2 (t2g)6
未成对电子数: 4 0
ptfe化学组成分析
在[Fe(CN)6] 4–中,CN–的配位原子为电负性较小的C,易给出电子对,对Fe2+的d电子排布影响大,Fe2+ 的6个单电子被挤到3个d轨道,空出2个d轨道,可用内层d轨道形成d2sp3杂化,内轨型,没有单电子,反磁性。用晶体场理论解释:在[Fe(CN)6]4– 中,CN– 为强场配体,分裂能大于成对能,没有单电子,反磁性。
铁磁性物质有永久磁矩吗
顺磁性表示此物质中有未成对的电子,反磁表示电子全部成对。Fe(II) 电子组态:3d6
价键理论:
[Fe(H2O)6]2+ [Fe(CN)6)]4-
杂化: sp3d2 d2sp3
未成对电子数: 4 0
晶体场理论:
弱场 (高自旋) 强场 (低自旋)
电子排布: (t2g)4(eg)2 (t2g)6
未成对电子数: 4 0
fe电子层为什么不稳定
[Fe(CN)6]3-和[Fe(CN)6]4都是内轨型络合物,都是采用d2sp3杂化,但二价铁离子d轨道有6个电子,分占三个d每个轨道有两个电子,都是配对的,所以磁矩为零;而三价铁离子中d轨道有5个电子,分占三个d轨道,其中有一个轨道只有一个电子,所以磁矩不等于零。